
14-3-3 / H+-ATPase model peptide / フシコクシン 三者会合体の概念
研究概要
医薬品の多くは,疾病にかかわる酵素の活性サイトを標的として開発されて来きました.もちろんこの手法は,少なくとも近未来的には主要な創薬手法であり続けるでしょう.しかし,たとえば,遺伝子発現に至る細胞内信号伝達経路上において,多くのたんぱく質?たんぱく質相互作用が関与しているという事実からすれば,この相互作用の制御も標的となりえるはずであり,実際そうした研究展開の重要性が指摘されつつあります.
私たちのグループでは,主にコチレニン(CN)およびフシコクシン(FC)というジテルペン配糖体に注目し、構造生物学の成果として提出されるたんぱく質の3次構造を「眺め」,論理的に分子設計を行い、有機合成駆使して,上記相互作用を制御し得る有機低分子化合物を創出すべく研究を行っています.

14-3-3 / H+-ATPase model peptide / フシコクシン 三者会合体の概念
コチレニン/フシコクシン
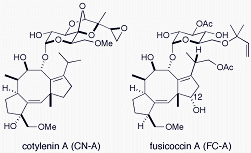
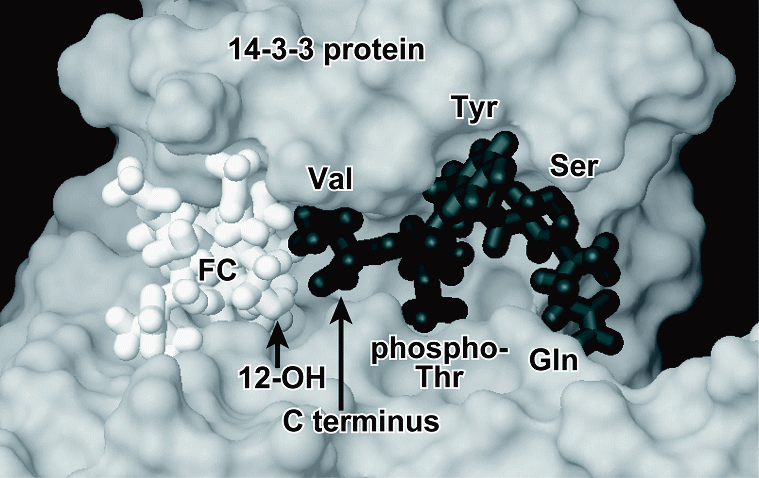
ジテルペン配糖体であるコチレニン(CN)およびフシコクシン(FC)は,休眠種子の発芽を強力に誘起するなど,特異な植物ホルモン様活性を持つことで古くから知られていました。この活性は,植物形質膜状のH+-ATPaseのC末端リン酸化部位と14-3-3たんぱく質の会合安定化に起因しており,下図に示すように14-3-3たんぱく質/リン酸化ペプチド/FC3者会合体の結晶構造も明らかにされています.この活性発現機構および3者会合体の構造は極めて興味深いものです.すなわち,
i) 14-3-3たんぱく質は,真核細胞生物の広範な細胞内に普遍的に発現し,Ser/Thrキナーゼによってリン酸化される多くのたんぱく質と会合体を形成することで,細胞内信号伝達を制御していること,
ii) CN/FCは14-3-3たんぱく質とリン酸化されたH+-ATPaseの2者会合体が形成するクレフトに,いわばジグソーパズルの3つ目のピースとして嵌り込み,安定な3者会合体を形成していること,
以上の2点において特に興味がもたれます。i) の事実は,植物のみならず,動物細胞内でもCN/FCが14-3-3たんぱく質の機能制御を通して何らかの活性を示す可能性を示唆します。一方,ii)
は,CN/FCがたんぱく質?たんぱく質相互作用を増強している、つまり正のモデュレーターとして機能していることに他なりません。近年になってタンパク質間の相互作用を阻害する研究は注目を集めて来ていますが、タンパク間相互作用を正にモデュレートする研究はあまり行われておらず、この点からもFC/CNは非常に魅力的な化合物と言えます。私達はFC/CNに焦点を当て、
A)創薬化学、B) フォワードケモゲノミクスC) リバースケモゲノミクス、D)生合成経路の解明と半構築半合成法の確立の4つを柱として研究に取り組んでいます。
A) 創薬化学
恐らく上述の発現機構と関連すると考えていますが,近年、CNはヒト白血病細胞に対して細胞分化誘導活性を示すことが明らかになりました。しかも,単剤としての血液系腫瘍に対する分化誘導活性だけではなく,インターフェロンαと併用すると各種固形癌に対してアポトーシスを誘導し,顕著な腫瘍増殖抑制効果示す.ヌードマウスへのヒト卵巣癌の異種移植片に対しても,毒性を示すことなく高い確率で完全治癒をもたらしました。しかし,少なくともHL-60に対する分化誘導活性はCNに特有のもので,植物に対しては同等の活性を有するFCは全く異なる活性を示します。我々は,得意とする有機合成化学を用いてFC誘導体を合成し、その構造活性相関研究を通じて、新規抗がん剤に関する創薬研究を行っています。その結果、これまでにCNと同等の分化誘導活性を示すISIR005などを見出しています。

B)抗がん活性における作用機序の解明; フォワードケモゲノミクス
上述のように優れた抗がん活性を有するCNですが、その作用機序は未だ明らかにされていません。我々はこれを明らかにするため、1つの仮説、即ち、“CNの抗癌活性の発現は14-3-3たんぱく質を介したシグナル伝達のモジュレーションによりに発現される”ことを想定し研究を進めています。既に述べたように、14-3-3たんぱく質はヒトにおいても発現され、14-3-3タンパク質と会合体を形成するリン酸化たんぱく質は200以上あると言われています。これらの中には、細胞周期や、アポトーシスに関わるものも多く報告されているため、抗がん活性が14-3-3を介したものであるという仮定は決して無理なものではなく、実際にインターフェロンαとの併用による各種固形癌の増殖抑制活性には14-3-3が関わっていると示唆するデータを得ています。現在は、14-3-3と結合するリン酸化タンパク質の内、どれがCNの抗がん活性に関わっているのかをウェスタンブロットやsiRNA等の生化学的手法を用いて明らかにしようとしています。
C) リバースケモゲノミクス
フォワードケモゲノミクスでは、抗がん活性のある分子をプローブとして、そこからその活性の由来を調べて行くという流れで研究が進めています。しかし、これとは逆に、ある特定の配列と3者会合体を形成するプローブ分子をあらかじめ創出しておき、このプローブ分子を細胞等に投与したときに現れる効果を詳しく調べることで、その機能を明らかにするリバース方向の研究も可能です。これを実現するにはターゲットとなるリン酸化たんぱく質の配列に応じて、これと上手く3者会合体を形成するような分子をデザイン、合成しなければならなりません。我々はコンピューターを用いたドッキングシミュレーションや精密有機合成、及び共同研究者であるC.
Ottmann博士(ドイツ マックスプランク協会・ケミカルゲノミクスセンター)の協力によって3者会合体のX結晶構造解析を行うことで、この課題を克服しようとしています。
D)半構築半合成法
触媒的クロスカップリングやオレフィンメタセシスの登場など、近年、有機合成化学は目覚しい発展を遂げています。とは言え、多官能基化された複雑な天然物を全合成するのは現代有機化学の力を以てしても容易なことではありません。上記の研究では、主に菌体から生産される天然物を原料として、半合成的手法によって誘導体を合成してきました。天然物を原料に用いるメリットはその化合物の骨格が既に出来上がっていることにあります。しかし、それ故に誘導体の変換反応が限られてしまう、即ち、任意の位置に望む官能基を導入するのが難しいという欠点もはらんでいます。この問題を解決するための一つの方法論として、我々は逆構築半合成法を提案しています。即ち、然るべき位置に目的の官能基などを含んだ擬生合成中間体を有機合成によってあらかじめ合成しておき、この擬中間体を菌体などの生体に“代謝”させることで目的の化合物を得る方法です。従来の半合成法の“生合成→化学合成”とは逆に、“化学合成→生合成”という手順を踏むことが特徴で、この方法では有機合成が得意とする骨格構築を化学合成で、それに続く高度な官能基化は生体に行わせることで目的の化合物を効率よく創出することが出来きます。既に本手法によってフッ素含有FC誘導体を合成することに成功しています。また、本手法が適用可能な基質を推測するためにFC、CNの生合成経路の解明にも取り組んでいます。
その他
この他にも多剤耐性バクテリアが発現する薬剤排出ポンプなど,幾つかの異なる標的を対象とした創薬研究や,細胞から放出されるスフィンゴシンの定量法の開発、医薬候補化合物の合成プロセスの確立に関する研究等,多岐に亘る研究テーマに取り組んでいます。