[ 血中ビリルビン濃度を高感度に測定する化学発光センサー ]
( Yukino Itoh, Mitsuru Hattori, ACS Sensors )
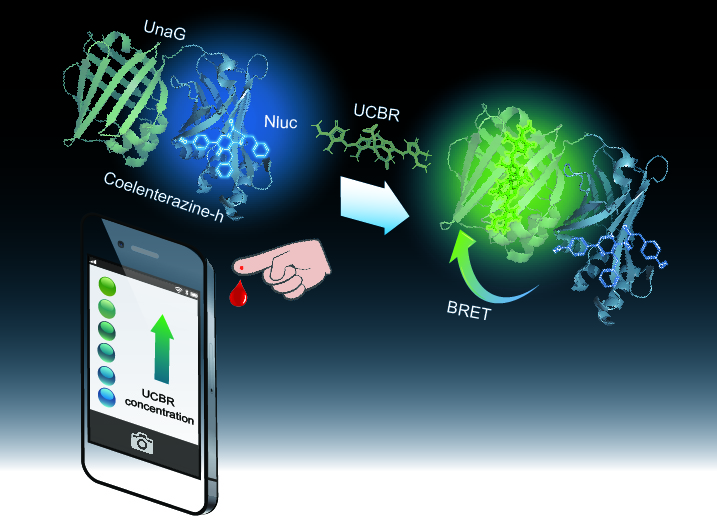
黄疸の原因分子であるビリルビンに対して、わずかな血液から簡単に血中ビリルビン量を計測できる生物発光指示薬「BABI (ベイビー)」を開発しました。ヘモグロビンの代謝産物である非抱合型ビリルビン (UCBR) は、新生児においてその血中濃度が過剰になりやすく、重症な場合には核黄疸 (ビリルビン脳症) による脳障害をもたらします。さらに近年、早産児の増加により黄疸は重症化しやすくなっているため、高感度な血中UCBR測定の重要性が増しています。BABIはUCBRが結合すると発光色が青から緑へと変化する性質を持つため、その色変化を定量することでUCBR濃度を計測することができます。またこの発光色変化は目視で確認できるほど明瞭であるため、スマートフォンカメラのような汎用カメラを用いて撮影することが可能です。実際に成分を調整したマウス血液を用いてヒト新生児の血液を模倣し、BABIによって全血中のUCBR濃度が測定可能かを検証しました。その結果、3 µLのマウス血液をBABIと混合し、その発光をスマートフォンカメラで撮影するという単純な手順でUCBR濃度の計測が可能であることが示されました。BABIは非常に高い検出感度を有するため、黄疸の症状である皮膚や眼の色が変化する前でも、その予兆を早期検出することが可能となります。本システムは、場所を選ばず、専門的な技術も必要としないため、誰でも知りたいときに手軽に計測できる手段として、将来のポイントオブケア診断における計測プラットフォームへと展開が期待されます。

[ "生物発光膜電位センサー"を用いた脳活動ライブ計測法の開発 ]
( Shigenori Inagaki, Scientific Reports, 9, 7460, 2019 )
私たちの脳では、神経細胞が回路を形成し、電気的な信号の伝搬を通じて認知・行動・記憶といった高次脳機能を実現します。それら脳機能を詳細に理解するために、従来は電極を用いた脳活動計測が行われてきました。しかしこの手法では、特に自由行動中の動物における脳活動を計測する際に、それぞれのマウスにケーブルを接続する必要があります。したがって、例えば社会性行動を行っている複数のマウスから同時計測を行おうとすると、ケーブルが絡まってしまうことなどが問題となり、研究が困難でした。 そこで、今回我々は「生物発光膜電位センサー LOTUS-V」を利用した新規脳活動計測法を開発しました。LOTUS-Vが神経活動に応じてその発光色を変化させることを利用して、ミリ秒単位で変化する脳活動の計測ができます。生物発光を利用することで、夜にホタルの光を撮影するように、LOTUS-Vの色の変化を離れた場所からでも検出できます。このワイヤレスなライブ脳活動計測技術により、世界で初めて自由行動中の複数マウスからの同時計測が可能になりました。 そして、この計測法を用いて実際にマウスが他のマウスと接触する際の脳活動を観察したところ、一次視覚野の神経活動が接触に応じて優位に上昇することを世界で初めて発見できました。これは今回開発された計測法が、未知の脳機能を発見する手段として有用であることを示唆しています。特に、これまで研究が困難であった、複数動物間のコミュニケーションなどの社会性行動を司る脳機能の解明、そして関連する自閉症スペクトラムや対人恐怖症などの精神疾患の研究・治療への貢献が期待されます。
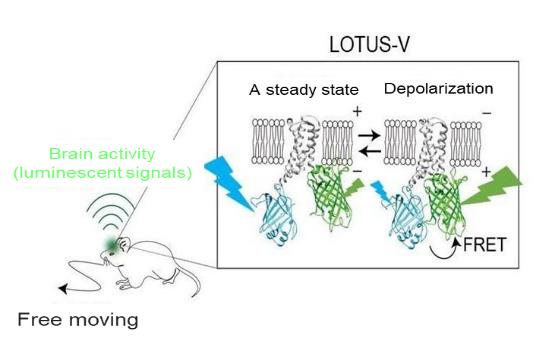
ワイヤレス脳活動計測の概略図。LOTUS-Vが導入された脳領域からの発光色の変化を計測する。LOTUS-Vは発光タンパク質( 水色 )、蛍光タンパク質( 黄緑色 )、膜電位感受性ドメイン( 灰色 )からなる融合タンパク質。脱分極した際、膜電位感受性ドメインが構造変化を起こし、発光タンパク質と蛍光タンパク質間の距離が近くなる。そしてFRETと呼ばれるエネルギー移動の効率が上昇し、黄緑色の発光が増強される( 水色の発光は減衰する )。
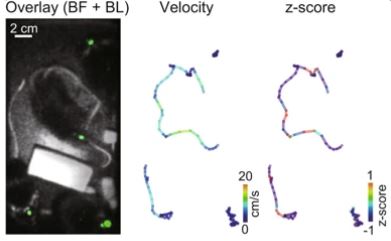
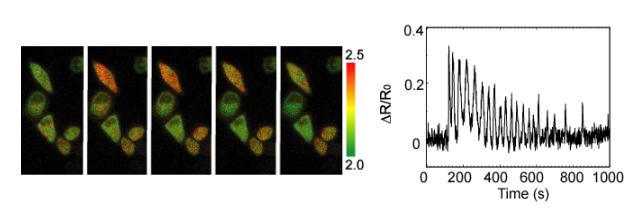
4匹のマウスにおける一次視覚野からの発光シグナル( 緑 )( 左側 )、マウスの移動速度( 中央 )、及び脳活動度( 右側 )( 標準化された黄緑色/水色発光レシオ値 )をそれぞれ疑似カラーにより可視化、時間ごとに変化する様子を移動の軌跡とともに示した。
[ 単一分子を検出可能な5色の高光度化学発光タンパク質の開発 ]
( Kazushi Suzuki, Nature Communications, 7, 13718, 2016 )
酵素活性の高い化学発光タンパク質と5種類の異なる蛍光タンパク質をハイブリッド化することにより、従来のものより2倍から10倍明るく、水色、緑色、黄緑色、橙色、赤色に発光するタンパク質enhanced Nano-lantern ( 増強型ナノ・ランタン )を開発しました。5色の増強型ナノ・ランタンが完成したことにより、細胞内の5つの微細な構造を同時に計測することに成功しました。また、増強型ナノ・ランタンを用いることで、1個単位のタンパク質分子の結合・解離を化学発光で検出することに世界で初めて成功しました。これまで、このような計測は蛍光タンパク質を用いて真夏の日光の何倍もの強度の光を照射しながら行われており、自家蛍光や光毒性の影響が問題になっていました。増強型ナノ・ランタンは、外部からの励起光を必要としないため、自家蛍光や光毒性の影響を全く受けません。 さらに、増強型ナノ・ランタンを改変して細胞内カルシウムイオンを検出できる化学発光型センサーも開発し、iPS細胞由来の心筋細胞で60枚/秒という高速度で長時間にわたってイメージングすることにより、忠実なカルシウムイオン動態の計測にも成功しました。これら化学発光型センサーは、細胞をより生理的な状態で実時間計測することを可能にし、生命科学研究のみならず、医学・薬理学研究に大きな貢献が期待されます。また、高光度かつ組織透過性に優れた増強型ナノ・ランタンの赤色変異体は、体の深部にあるシグナルを体外から感度良く観察することができます。従って、がん幹細胞などの体外からの観察が可能になるため、多くの疾病の原因究明やより効果的な創薬スクリーニングが期待されます。

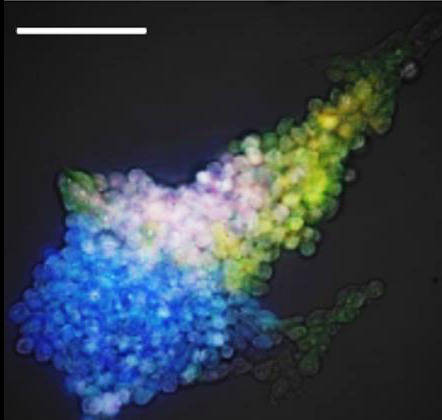
試験管に入れた5色の増強型ナノ・ランタンに発色物質ルシフェリンを添加し撮影
[ 青緑( シアン )色およびオレンジ色の超高光度発光タンパク質の開発 ]
( Akira Takai, Proc. Natl. Acad. Sci. USA, 112, 4352-4356, 2015 )
2012年に開発した黄緑色の超高光度発光タンパク質Nano-lantern( ナノ・ランタン )を改良して、さらに明るく光る青緑( シアン )色およびオレンジ色の超高光度発光タンパク質の開発に成功しました。いずれも従来の発光タンパク質の20倍程度明るく光るため、特殊な超高感度カメラを使わなくとも、肉眼やスマートフォンのカメラでその発光を観察することが出来ます。
また、3色の色違いのナノ・ランタンが完成したことにより、細胞内の微細な構造の動態や遺伝子の発現を複数同時に計測することが初めて可能となり、万能細胞( ES細胞 )の万能性維持に重要な3つの遺伝子の発現の様子を同時に観察することに世界で初めて成功しました。万能細胞の研究では、蛍光タンパク質を用いる際の自家蛍光や光毒性の影響が問題となっていました。ナノ・ランタンは、外部からの励起光を必要としないため、自家蛍光や光毒性の影響を全く受けません。従って、再生医療の研究において大きな貢献が期待されます。
さらに、ナノ・ランタンを改変して細胞内カルシウムを検出できるシアンおよびオレンジ色の発光指示薬の開発に成功しました。これらの発光指示薬は、外部からの照明光を必要とせず自ら発光するため、光で細胞の活動やタンパク質の機能を制御する光遺伝学的技術との組み合わせが容易です。神経活動の操作と計測を同時に行うことが可能となり、脳のメカニズムの研究への応用が期待されます。蛍光タンパク質は、最初の緑色から、青緑色、続いてオレンジ~赤色と3色揃うことで急速に応用が拡大しました。蛍光タンパク質に比肩しうる明るさで光る超高光度発光タンパク質ナノ・ランタンが青緑色、黄緑色、オレンジ色と3色揃ったことで、同様に利活用が進展するものと期待されます。
なお、この研究は理化学研究所生命システム研究センターの岡田康志チームリーダーらの研究チームと共同で行われました。

[ 超高輝度発光たんぱく質Nano-lantern( ナノ-ランタン )の開発 ]
( Kenta Saito, Nature communications, 3, 1262, 2012 )
蛍光タンパク質を中心とした蛍光プローブの普及に伴い、生物個体を生きたまま可視化するライブイメージング技術が著しい発展を遂げています。観察対象が様々な動植物種に広がる一方で、蛍光観察におけるサンプルへの光毒性や自家蛍光といった問題が浮上してきました。
これらの問題を回避するために、我々の研究グループではホタルに代表される「化学発光」を用いたライブイメージングに取り組んできました。化学発光は蛍光と違い外部からの励起光を必要としないため、自家蛍光や光毒性といった問題を回避することができます。このような利点があるにも関わらず化学発光は蛍光に比べて明るさが足りないという弱点があったため、ライブイメージングの道具として有用ではありませんでした。例えば従来の化学発光でマウス体内の癌細胞を検出する場合は、麻酔で眠らせたヌードマウスを暗い環境で、長時間露光撮影する必要がありました。
今回我々は、化学発光タンパク質と蛍光タンパク質をハイブリッド化することで、従来の化学発光プローブに比べ10倍以上明るい超高輝度化学発光タンパク質 Nano-lantern( ナノ-ランタン )を開発しました。Nano-lanternを用いることで、自由に動き回るマウスの背中で光る癌細胞の様子をビデオレートで撮影することに世界で初めて成功しました。特別な処置すること無くマウスを化学発光で観察できるので、多くの疾病の原因究明やより効果的な創薬スクリーニングが期待されます。さらに我々は、Nano-lanternを改変してCa2+やcAMP、ATPを検出できる発光プローブの開発にも成功しました。これらの発光プローブは励起光を必要としないため、植物細胞のような自家蛍光の強い試料における活性測定や、光照射により細胞の活動やタンパク質の機能を制御する「光遺伝学的技術」と組み合わせて用ることが容易です。例えば、神経ネットワークのコントロールと神経活動のモニタリングを同時に行うことができるため、複雑で実験が困難であった高次神経活動( 行動、思考、記憶 )のメカニズムに迫ることが可能となります。

[ 化学発光性カルシウムイオン指示薬"BRAC"の開発 ]
( Kenta Saito, PLoS ONE, 5: e9935,2010)
FRETや蛍光タンパク質を用いた「蛍光観察」ではサンプルへ強い励起光を当てる必要があります。 そのため励起光が届きにくい生物個体内部や、自家蛍光が多くまた光毒性の影響が多い植物等への適用は難しい点もあります。 一方、ホタルの光のように励起光を必要とせずに発光を起こす生物発光タンパク質も同定され研究に利用されています。 我々はこのように励起光を必要としない「発光観察」を生物個体へのイメージングにアプローチしようとしています。 生物発光タンパク質から蛍光タンパク質へのBRET( Bioluminescene Resonance Energy Transefer )を利用したバイオセンサーの開発も行っています。 新規に開発した発光性Ca2+指示薬BRACを発現したHela細胞のカルシウム振動を観察を行いました。
GLICO
Under construction
CeNL( Ca2+ )/OeNL( Ca2+ )
Under construction

 NAGAI Laboratory
NAGAI Laboratory