ポイント
- 最初にウイルス感染した細胞からのメッセージを周囲の非感染細胞が受け取ることを発見。
- メッセージを受け取った非感染細胞は感染しやすくなり周囲へのウイルス感染を加速。
- メッセージのやり取りを標的とした新しい概念の創薬・治療に期待。
概要
北海道大学大学院医学研究院の藤岡容一朗准教授、小澤史弥氏、大場雄介教授、大阪大学産業科学研究所(兼 大阪大学先導的学際研究機構)の永井健治教授、九州大学大学院医学研究院の田村友和准教授と福原崇介教授らの研究グループは、インフルエンザウイルスが体の中で感染を広げていく際に、細胞同士の“会話”を乗っ取ることを突き止めました。この発見により、ウイルス感染を抑える新たな治療法の開発が期待されます。
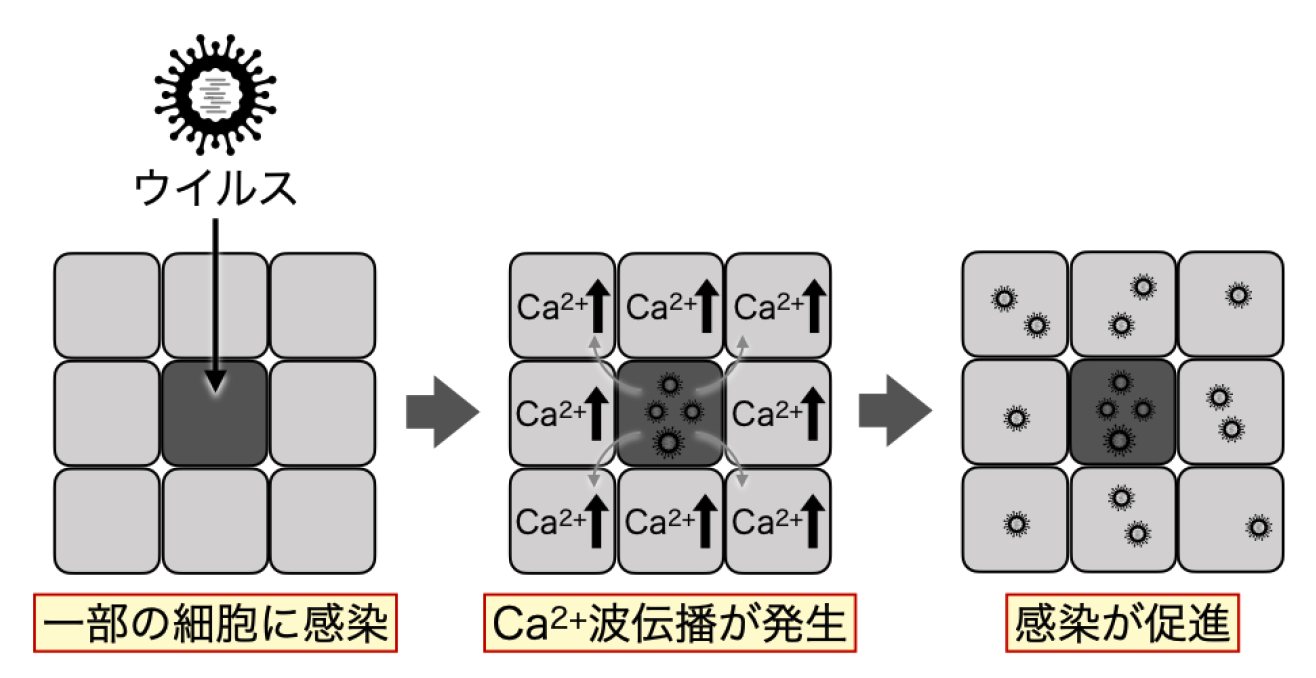
ウイルス感染は、ごく一部の細胞から始まり、徐々に周囲の細胞へと広がっていきます。しかし、感染がどのように周囲の細胞に広がっていくのか、その詳細なメカニズムはよく分かっていませんでした。
研究グループはこれまでに、細胞内のカルシウムイオン濃度が上昇すると、インフルエンザウイルスが感染しやすくなることを突き止めています。今回の研究では、ウイルスに感染した細胞が「ADP(アデノシン二リン酸)※1」を細胞外に放出し、それを周囲の細胞が受け取ると細胞内カルシウムイオン濃度が上昇することを、超広視野高解像顕微鏡AMATERAS※2等を用いた解析により発見しました。この現象は“カルシウム波伝播”と呼ばれ、まるで伝言ゲームのように次々と隣接する細胞へと連鎖的に広がっていきます。今回の研究で、この“カルシウム波伝播”の仕組みをウイルスが乗っ取り、感染を加速させていることが分かりました。さらに研究グループは、「ADP受容体※3」をブロックすることで、この波の伝播を止め、感染が抑えられることも示しました。
本研究成果は、ウイルスがどのように体の中で広がるのかという謎を解くだけでなく、将来的には「細胞同士の会話」を標的とした、新しいウイルス治療薬の開発にも繋がる可能性があります。
なお、本研究成果は、日本時間2025年8月2日(土)公開のCell Communication and Signaling誌にオンライン掲載されました。
背景
ウイルスは、体の中のごく一部の細胞に感染し、そこから周りの細胞へと感染を広げていき、最終的に広範囲に感染します。しかし、どうやって少数の感染細胞から周囲に感染が広がっていくのか、その仕組みはよく分かっていませんでした。これまで研究グループは、細胞内のカルシウムイオンの濃度が高くなると、ウイルスが感染しやすくなることを明らかにしてきました。
そこで今回は、細胞内カルシウムイオン濃度の変化に注目し、ウイルスがどのように体の中で感染細胞を増やしていくのかを詳しく検証しました。
研究手法
研究グループは、一度に数十万〜百万個の細胞を同時に観察できる顕微鏡を使って、ウイルスに感染した際に細胞のカルシウムイオン濃度がどのように変化するのかを解析しました。また、カルシウムイオン濃度変化を抑える薬がウイルス感染を抑えるかどうかを検証しました。
研究成果
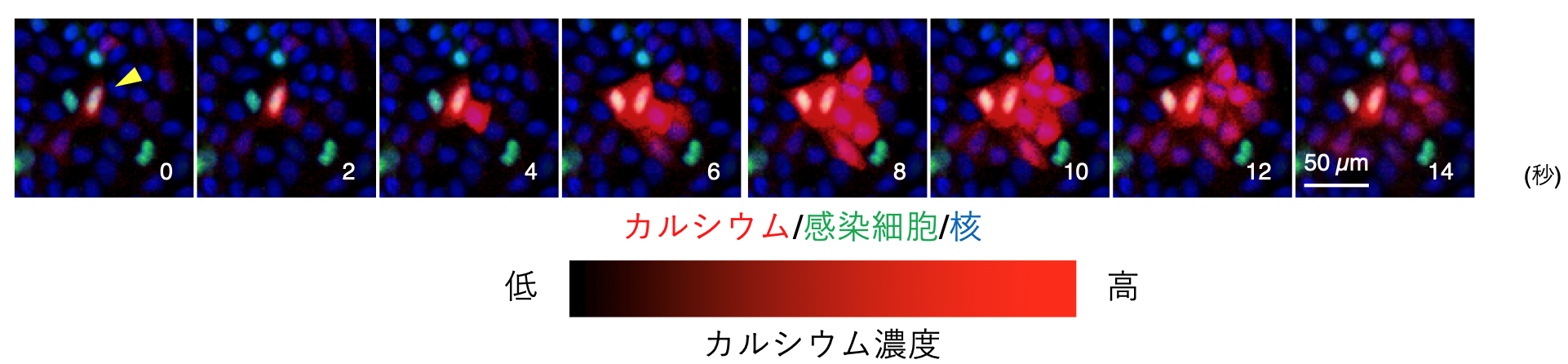
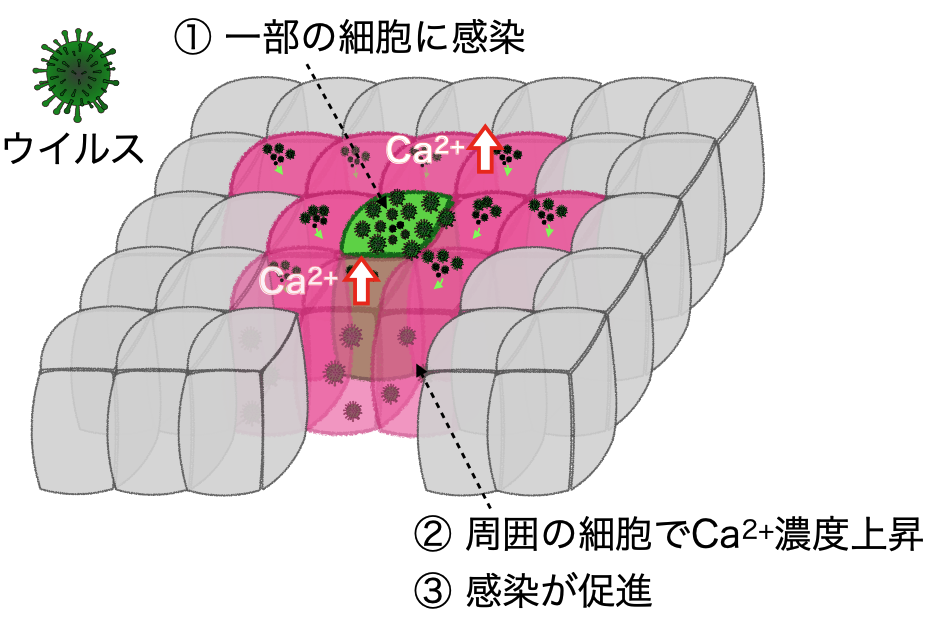
ウイルス感染時の細胞集団レベルでのカルシウムイオン濃度変化を超広視野高解像顕微鏡AMATERAS等により観察したところ、感染細胞を起点として、周囲の細胞にカルシウムイオン濃度上昇が波のように伝播する現象(カルシウム波伝播)を発見しました(図1、図2)。感染細胞から放出された「ADP(アデノシン二リン酸)」を周囲の細胞が「ADPの受容体」を通して受け取ることで、細胞内カルシウムイオン濃度が上昇することが分かりました。
すなわち、感染細胞と周囲の非感染細胞は、ADPとADP受容体を使って、会話していたのです。
また、ADP受容体をブロックする薬を細胞に処理すると、感染が抑えられました。同じ薬をマウスに投与しても感染の抑制が確認され、「カルシウム波伝播」が生体内でもウイルスの感染拡大に重要な役割を果たしていたことが示されました(図3)。
今後への期待
本研究により、“感染した細胞”と“まだ感染していない細胞”の間の会話(ADP)をウイルスが利用し、“まだ感染していない細胞”が感染しやすくなることが分かりました。「ウイルスそのもの」を標的とした薬は、ウイルスが薬に対して耐性を獲得するリスクがありますが、この「細胞同士の会話(ADP)」を治療標的とすることで、そのリスクを減らせると期待されます。今後、この研究成果をもとに新しい概念に基づく抗ウイルス薬の開発が進むことが望まれます。
謝辞
本研究はMEXT科研費JP20H05872、JP15H01248、JP26115701、JP19H05411、JP19H04823、 JP21H00413、JSPS科研費JP21H02735、JP24K02255、JP24K22042、日本医療研究開発機構(AMED)革新的先端研究開発支援事業JP20fk0108401、JP21gm1610001、持田記念医学薬学振興財団・コニカミノルタ等からの助成を受けたものです。
論文情報
論文名:The crucial role of intercellular calcium wave propagation triggered by influenza A virus in promoting infection(細胞間カルシウム波伝播によりインフルエンザウイルス感染が促進される)
著者名:小澤史弥1、田村友和2(研究当時)、6(研究当時)、7(研究当時)、8、高橋直希1、垣塚太志3、市村垂生4、島田琉海1、橋本泰行1、鬼塚洋之進1、柏木彩花1、釜崎とも子1、天野麻穂1、永井健治3、4、5、福原崇介2(研究当時)、6(研究当時)、7(研究当時)、8、藤岡容一朗1、大場雄介1(1北海道大学大学院医学研究院細胞生理学教室、2北海道大学大学院医学研究院病原微生物学教室、3 大阪大学産業科学研究所、4 大阪大学先導的学際研究機構、5北海道大学電子科学研究所、6北海道大学ワクチン研究開発拠点、7北海道大学One Healthリサーチセンター、8九州大学大学院医学研究院ウイルス学分野)
雑誌名:Cell Communication and Signaling(細胞生物学の専門誌)
DOI:10.1186/s12964-025-02357-y
公表日:2025年8月2日(土)(日本時間、オンライン公開)
参考図

用語解説
※1 ADP(アデノシン二リン酸)
細胞内でエネルギーのやり取りに関わる物質であり、ATP(アデノシン三リン酸)が利用されることでリン酸基が一つ外れ、ADPが産生される。
※2 AMATERAS
正式名称はa multiscale/modal analytical tool for every rare activity in singularity。大阪大学産業科学研究所の永井健治教授(兼 大阪大学先導的学際研究機構 教授)、垣塚太志特任研究員(常勤)、大阪大学先導的学際研究機構の市村垂生特任准教授(常勤)らが開発した、超広視野高解像顕微鏡。
※3 ADP受容体
細胞の表面(細胞膜)に存在するタンパク質で、ADPに結合すると他のタンパク質と協働して、細胞内のカルシウムイオン濃度を上昇させる。

