-セルロースナノファイバーを用いた唾液中のがん由来エクソソーム解析プラットフォームを開発-
ポイント
- 唾液中のエクソソーム由来のmicroRNAを網羅的に解析し、がんリスクモニタリングとしての可能性を提示
- セルロースナノファイバーからなるシート型デバイスで、極微量(0.01 mL)の唾液からエクソソーム由来microRNAを抽出
- 日常的な唾液採取によるがんリスクモニタリングなど、個別化医療・予防医療への応用に期待
概要
東京科学大学(Science Tokyo)生命理工学院 生命理工学系の安井隆雄教授、阿尻大雅助教と大阪大学 産業科学研究所の古賀大尚准教授らの研究チームは、日常的に採取可能な唾液からエクソソーム※1由来のmicroRNA※2を網羅的に解析し、がん診断ツールとしての可能性を示しました。
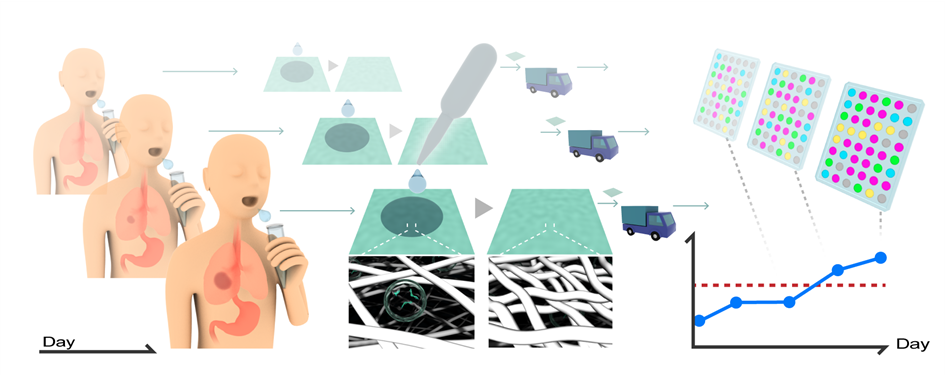
がんの早期発見や治療効果のモニタリングには、負担の少ないリキッドバイオプシー※3の活用が期待されています。その中でも唾液は、採取が簡便で繰り返し検査しやすいことから、日常的な健康チェックに適した検体として注目されています。本研究チームは、唾液中のエクソソームと呼ばれる、細胞が分泌する微粒子に含まれるmicroRNAに着目し、がん診断・がんリスク評価の新たなツールとして利用できる可能性を検証しました(図1)。
本研究では、セルロースナノファイバー(cellulose nanofiber:CNF)※4からなるシート状のデバイスを用い、極微量(0.01 mL)の唾液からエクソソーム由来microRNAを効率よく回収できる手法を開発しました。本デバイスと、従来広く用いられている回収方法である超遠心法を比較したところ、同量の唾液を出発材料とした条件下で、CNFシートはより高いmicroRNA回収能を示しました。また、超遠心法などの従来の回収方法では、回収後のエクソソームを-80℃で保存することが求められますが、本手法ではシートの乾燥操作により、長期間(1週間以上)室温での保存が可能となりました。
さらに、健常者と肺がん患者・胃がん患者から採取した唾液を用いてmicroRNAの発現プロファイルを解析した結果、がん患者群では健常者とは異なる特徴的な発現パターンが得られ、本手法ががん関連microRNAの検出やバイオマーカー候補の探索に有用であることが示されました。本研究で開発したCNFシートを用いることで、採血を伴わず、少量の唾液と簡便な操作でエクソソーム由来microRNAを評価できるため、将来的には自宅や地域医療の現場における日常的ながんリスクモニタリングや、個々の患者の病勢変化を追跡する個別化医療への応用が期待されます。
本成果は、1月22日付(現地時間)の「Biosensors and Bioelectronics」誌に掲載されました。
背景
がんは日本を含む世界各国で主要な死因の一つです。その治療成績が「どれだけ早くがんを見つけられるか」に大きく左右されるため[参考文献1]、負担の少ない方法で日常的に体の変化をモニタリングできる技術が求められています。その一つとして注目されているのが、血液などの体液中の分子の情報を解析するリキッドバイオプシーです。体液中にはさまざまな分子が含まれますが、なかでも遺伝子の働きを微調整する小さなRNAである「microRNA」はヒトでは2,500種類以上が存在するとされ、すでにさまざまながんでmicroRNAの増減パターンが変化することが知られています。特に細胞が放出するナノサイズの微粒子であるエクソソームに包まれたmicroRNAは、酵素分解に比較的強く、有望なバイオマーカー※5として世界的に研究が進んでいます[参考文献2]。
このmicroRNAを調べるには、血液検査は有用であるものの、採血時の痛みや心理的な負担、衛生面の配慮などが、日常的なモニタリングを実現する上で大きなハードルとなります。一方で唾液は、痛みもなく、自宅でも繰り返し採取できる理想的な検体の一つです。ところが、タンパク質や粘液などの成分が多く、従来のエクソソーム分離法(超遠心法やクロマトグラフィーなど)を適用するには、これらを除去するための追加の前処理が必要となり、大型装置を用いた長時間の処理が避けられないという課題がありました[参考文献3]。また、得られたエクソソーム試料は-80℃での凍結保存が必要であり、「日常的に測る」といった使い方には適していませんでした。
そこで研究チームは、唾液中のエクソソーム由来 microRNA を簡便に取り出し、室温で安定に保存・解析できる方法の開発に取り組みました。研究チームはこれまでに、セルロースナノファイバーからなるシート状デバイス(CNFシート)を用いたエクソソーム回収技術を開発しており[参考文献4]、本研究ではこの CNF シートを唾液に応用し、その有用性を検証しました。
研究成果
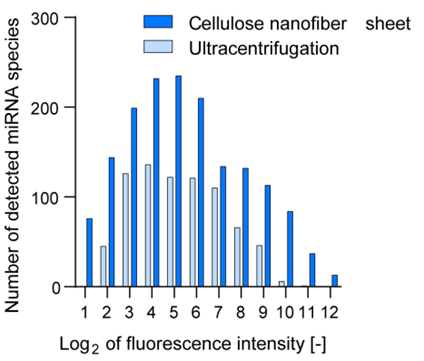
はじめに、エクソソームの捕捉に適した細孔径分布(約4~300 nm)を持つCNFシートを設計しました。次に、CNFシートへの唾液滴下量を検討した結果、わずか0.01 mLの唾液を滴下するだけで、CNFネットワーク由来の細孔内にエクソソームが効率よく捕捉されることを見いだしました。また、唾液を滴下したCNFシートを乾燥させると、CNFネットワーク構造が収縮し、捕捉されたエクソソームを包み込むように固定するので、エクソソーム内部のmicroRNAが室温でも安定に長期間保存されることを明らかにしました。乾燥させたCNFシートを回収用溶液に浸漬すると、CNFネットワーク構造が再び緩み、エクソソームを抽出できることも確認しました。さらに、従来広く用いられている超遠心法とmicroRNAの回収効率を比較したところ、同量の唾液を用いた条件において、CNFシートを用いた方法ではより多くの種類のmicroRNAを検出できることが確認されました(図2)。
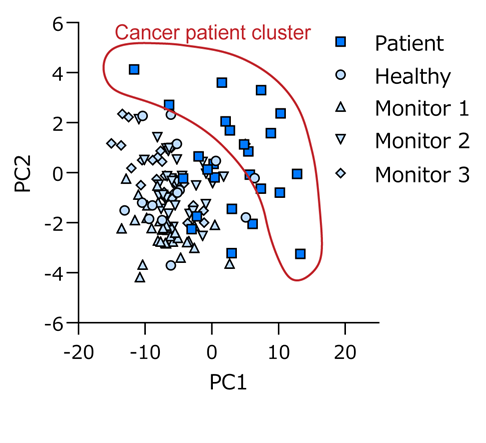
この手法の有用性を検証するために、肺がん患者、胃がん患者、および健常者から採取した唾液試料を用いてエクソソーム由来microRNAの発現パターンを解析したところ、がん患者群と健常者群の間で統計的に差がみられる「バイオマーカー候補となるmicroRNA」を発見しました。さらに、健常者から連日唾液を採取し、バイオマーカー候補のmicroRNA群について解析したところ、日常的な唾液採取・microRNA解析においても確かなデータの再現性と安定性を持つことも確認できました(図3)。これらの結果から、CNFシートを用いた本手法は、将来的ながん診断や日常的ながんリスクのモニタリングに向けた基盤技術として有望であることが示されました。
社会的インパクト
CNFシートによる唾液解析技術は、組織採取や採血を必要とせず、極微量の唾液からエクソソーム由来のmicroRNAを安定して評価できる点に特徴があります。がんに限らず、さまざまな疾患リスクを日常的にモニタリングし、一人ひとりの状態に合わせた個別化医療に貢献する技術としての活用が期待されます。
さらに、CNFシートを用いたエクソソーム回収技術は、必要サンプル量の少なさ、操作の簡便性、高い回収効率、室温での保存性など、従来のエクソソーム回収法には無い特徴を併せ持ちます。今後はリキッドバイオプシーとしての応用に加え、基礎から臨床応用まで、幅広いエクソソーム関連研究および事業への応用が期待されます。
今後の展開
今後は、より多くの患者・健常者の検体を用いた検証を進め、臨床的な有用性を評価していきます。さらに、CNFシートの改良にも取り組み、エクソソームそれ自体、あるいはエクソソーム由来microRNAのためのより高性能な解析プラットフォームに発展させることを目指します。併せて、産学連携を通じて、CNFシートの量産プロセスや品質管理体制の検討を進め、実用化・社会実装に向けた基盤づくりを行っていきます。
付記
本研究成果は、科学技術振興機構(JST)CREST(JPMJCR2576)、創発的研究支援事業(JPMJFR2003)、AMEDムーンショット研究開発事業(22zf0127004s0902、JP22zf0127009)、新エネルギー・産業技術総合開発機構(NEDO)(JPNP20004)、JST AIP加速研究(JPMJCR23U1)、日本学術振興会 科学研究費助成事業 基盤研究(A)(JP24H00792)、研究活動スタート支援(JP24K23101)、野口遵研究助成金(NJ202308)の支援のもとで得られたものです。
参考文献
[1] Crosby, David, et al. "Early detection of cancer." Science 375.6586 (2022): eaay9040.
[2] Yasui, Takao, et al. "Unveiling massive numbers of cancer-related urinary-microRNA candidates via nanowires." Science Advances 3.12 (2017): e1701133.
[3] Iwai, Kazuya, et al. "Isolation of human salivary extracellular vesicles by iodixanol density gradient ultracentrifugation and their characterizations." Journal of extracellular vesicles 5.1 (2016): 30829.
[4] Yokoi, Akira, et al. "Spatial exosome analysis using cellulose nanofiber sheets reveals the location heterogeneity of extracellular vesicles." Nature Communications 14.1 (2023): 6915.
用語説明
※1 エクソソーム
細胞が分泌する直径100ナノメートル(nm)前後の小さな胞体。核酸(DNAやmessengerRNA、microRNAなど)やタンパク質といった細胞の情報を持つ分子を搭載して、細胞外へ放出され、生命に重要な機能を有する。
※2 microRNA
2024年のノーベル生理学・医学賞の受賞につながった物質。microRNAはタンパク質を作らない小さなRNAであるが、細胞や生体を制御していることが明らかとなっている。がん細胞が放出するエクソソームに含まれるmicroRNAは体内のがんに関連するサインであると考えられている。
※3 リキッドバイオプシー
血液や尿などの体液を用いることでがんなどの病気の検査を行う方法。身体の一部を切り取る方法(バイオプシー、生体検査)と比較して、侵襲性が低い。
※4 セルロースナノファイバー(cellulose nanofiber:CNF)
植物細胞壁から抽出できるナノサイズ(1 mmの百万分の1)の非常に細い繊維。軽量、高強度、大比表面積かつ持続可能なナノマテリアルとして注目を集めており、工場での量産や実用化も進んでいる。
※5 バイオマーカー:病気の有無や進行度、治療効果などを判断するための体内の物質や指標。
論文情報
掲載誌:Biosensors and Bioelectronics
論文タイトル:Routine monitoring of microRNAs in salivary exosomes using a cellulose nanofiber sheet
著者:Taiga Ajiri*, Min Zhang, Naoya Mizukami, Mikiko Iida, Shota Kawaguchi, Yurie Sekihara, Kunanon Chattrairat, Zetao Zhu, Yoshinobu Baba, Hirotaka Koga*, Takao Yasui*
DOI:10.1016/j.bios.2026.118436

