研究成果のポイント
・神経細胞の自己認識・非自己識別に関わる細胞接着タンパク質※1であるクラスター型プロトカドヘリンの相互作用を可視化する蛍光※2センサーIPADを開発。
・同一神経細胞に由来する神経突起間におけるクラスター型プロトカドヘリンの相互作用を世界で初めて可視化。
・神経細胞におけるクラスター型プロトカドヘリン相互作用の生物学的意義の解明に繋がる技術的前進。
・自閉症やてんかん等の脳疾患で見られる、自己神経結合を可視化するセンサー開発に繋がる可能性。
概要
大阪大学産業科学研究所生体分子機能科学研究分野の京卓志特任研究員(常勤)(JSTさきがけ専任研究者)、永井健治教授、松田知己准教授の研究グループは、同生命機能研究科心生物学研究室の星野七海特任研究員(研究当時。現在Tulane大学研究員)、八木健教授の研究グループとの共同研究により、神経細胞の自己認識・非自己識別に関わる細胞接着タンパク質であるクラスター型プロトカドヘリン(Pcdh)の相互作用をイメージングするための蛍光センサー「IPAD」を開発しました(図1)。これまで、細胞間相互作用や細胞間における細胞接着タンパク質の相互作用は可視化されてきましたが、細胞の自己認識に関わるような、同一細胞から伸びた突起間の相互作用は可視化されていませんでした。 研究グループは、Pcdhのアイソフォーム※3の1つであるPcdhα4を標的とし、その分子内にタンパク質間の可逆的な結合解離のイメージングが可能なddGFP※4という特別な2つの蛍光タンパク質※5のペアを挿入することで、世界で初めて同一神経細胞に由来する神経突起間における、Pcdhα4間相互作用の可視化に成功しました。この研究成果は、神経細胞におけるPcdh相互作用の生物学的意義に迫るための技術的な大きな一歩であるとともに、自閉症やてんかんなどの脳疾患に見られる自己神経結合を検出するための蛍光センサー開発を発展させる基盤となることが期待されます。 本研究成果は、米国科学誌「iScience」に、7月18日(火)午前1時(日本時間)に公開されました。
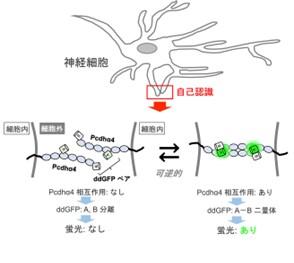
図1 IPADによる自己認識の検出
研究の背景
私たちが自分と相手を識別しているように、私たちの頭の中の神経細胞も自己と非自己を識別しています。これは一見同じように見える神経細胞にも個性があるということです。細胞接着タンパク質であるクラスター型プロトカドヘリン(Pcdh)は細胞表面を多様化させることで、神経細胞に個性を与えています。Pcdhには50種類以上のアイソフォームが存在し、1つ1つの神経細胞は、数種類から十数種類を異なる組み合わせで発現しています。細胞接着タンパク質としてのPcdhの面白い特徴は、同じ組み合わせのPcdhアイソフォームを発現する細胞間でのみ接着活性を示すということです。1つ1つの神経細胞は異なる組み合わせでPcdhアイソフォームを発現していることから、Pcdhは異なる神経細胞間では相互作用せず、同一神経細胞から伸びた突起間では相互作用するということが想定されています。これがPcdhを介した神経細胞の自己認識機構です。これまでPcdhの相互作用は、Pcdhを内在性の細胞接着タンパク質が発現していない血球細胞に発現させ、細胞同士が凝集するかどうかを観察することで解析されてきました。実際に同一神経細胞から伸びた突起間でPcdhが相互作用するのかどうかの直接的な証拠はありませんでした。この問題に取り組むために、神経細胞においてPcdh間の相互作用を可視化するための蛍光センサーを開発するという着想に至りました。
研究の内容
二量体形成によって蛍光を生じる特殊な蛍光タンパク質であるddGFPをPcdhのアイソフォームの1つPcdhα4の細胞外領域に挿入することにより、Pcdhα4相互作用によって緑色蛍光を生じる蛍光センサー「IPAD」を開発しました。これまで、細胞間相互作用や細胞間における細胞接着タンパク質を可視化するための蛍光センサーには、split-GFP※6という技術が使用されてきました。この技術を使用した蛍光センサーは、細胞が接触してから光り出すまでに時間を要するのに加え、反応が不可逆であるため、ダイナミックに変化する細胞間相互作用を捉えることが出来ませんでした。IPADでは、可逆的なddGFPを使用することで、同一神経細胞から伸びる突起間におけるPcdhα4相互作用の形成と解離をリアルタイムで捉えることに成功しました(図2)。
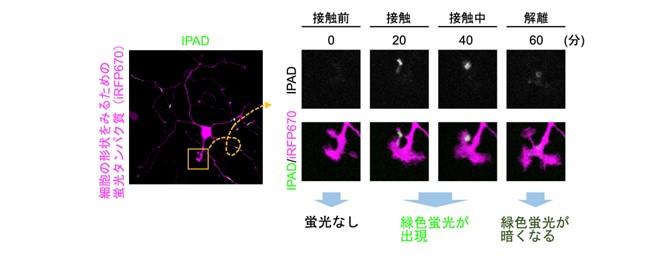
図2 IPADによる同一神経細胞から伸びる突起間におけるPcdhα4間相互作用の可視化
本研究成果が社会に与える影響(本研究成果の意義)
本研究において、同一神経細胞から伸びた突起間におけるPcdhの相互作用が初めて可視化されました。これまで、想定されてきた神経細胞の自己認識・非自己識別におけるPcdh相互作用の重要性を直接検討するための大きな一歩です。今後、IPADを使用して、その意義が明らかにされていくことが期待されます。
これまで、異なる細胞間の相互作用は様々な研究の対象になってきた一方、細胞の自己認識につながるような同一細胞の突起間相互作用は見過ごされてきました。本研究成果はこれまでほとんど注目されてこなかった同一細胞の突起間相互作用というものが、生物学的にどのような意義を有するのかという問いを投げかけるものでもあります。
Pcdhは自閉症などの発達障害、双極性障害や統合失調症などの精神疾患に対し感受性がある遺伝子として報告されています。今後、本研究成果の蛍光センサーを用いた解析を通して、これまでとは異なる視点からそれらの疾患を捉えることで、新たな病態メカニズムの同定につながる可能性があります。また、自己認識を可視化するために設計されたIPADのデザインを応用することで、自閉症やてんかんなどの脳疾患でしばしば見られる神経細胞の自己神経結合を可視化するツールの開発にもつながる可能性があります。
特記事項
本研究成果は、2023年7月18日(火)午前1時(日本時間)に米国科学誌「iScience」(オンライン)に掲載されます。
タイトル:"Visualization of trans-interactions of a protocadherin-α between processes originating from single neurons"
著者名:Takashi Kanadome*, Natsumi Hoshino* (*co-first), Takeharu Nagai, Takeshi Yagi, and Tomoki Matsuda
DOI:10.1016/j.isci.2023.107238
なお、本研究は、JST戦略的研究推進事業さきがけ「多細胞システムにおける細胞間相互作用とそのダイナミクス(JPMJPR2045)」、同CREST「細胞内現象の時空間ダイナミクス(JPMJCR20E4)」の助成を受けたものです。
用語説明
※1 細胞接着タンパク質:
細胞表面に発現し、細胞どうしの接着を仲介するタンパク質の総称。これまでに数百種発見されている。
※2 蛍光:
光を吸収し、その光よりも低エネルギー(長波長)の光を放出する物質の性質のこと。IPADは青色光(∼490nm)を吸収し、緑色光(∼510nm)を放出する。
※3 アイソフォーム:
機能はほとんど同じであるがアミノ酸配列が異なるタンパク質。
※4 ddGFP:
dimerization -dependent green fluorescent proteinの略。
ddGFP-AとddFP-Bからなる蛍光タンパク質。ddGFP-A単独では光らないが、ddFP-Bとヘテロ二量体を形成することで緑色蛍光を生じるようになる。IPADではPcdhα4間相互作用によりddGFP-AとddFP-Bが近づくとヘテロ二量体が形成される。この反応は可逆的であり、近年様々な蛍光センサー開発に利用されている。
※5 蛍光タンパク質:
蛍光を発するタンパク質の総称。2008年にノーベル化学賞を受賞した下村脩博士らが、1962年にオワンクラゲから初めて遺伝子を単離し、緑色蛍光タンパク質(Green Fluorescent Protein, GFP)と命名した。
※6 split-GFP:
2つのタンパク質間の相互作用を解析するために登場した技術で、GFPを2分割して得られる非蛍光性の断片のそれぞれを、解析対象のタンパク質に融合し、対象タンパク質間の相互作用に伴って再構成されたGFPから発せられる蛍光によってタンパク質間相互作用を検出する。
京特任研究員(常勤)のコメント
自己認識を可視化する蛍光センサー?何のこっちゃ?と思われる方が多いかもしれません。概念としては未熟ですが、世界のどこかにその重要性・面白さに気づいてくれる方がいるものと信じています。今回はPcdhの一つのアイソフォームを標的とした蛍光センサーを開発しました。今後は特定の細胞接着タンパク質を標的としたものでなく、より一般的に自己認識を可視化できるような蛍光センサーの開発を目論んでいます。

