研究成果のポイント
概要
大阪大学産業科学研究所のマータイン・ズワーマー特任准教授(常勤)、西野邦彦教授(兼 大学院薬学研究科/感染症総合教育研究拠点/微生物病研究所附属バイオインフォマティクスセンター)、櫻井希望さん(薬学部6年)、および米国セントルイス・ワシントン大学のヤン・ユ教授、米国インディアナ大学ブルーミントン校のスワガタ・バタチャーリャさんらは、新たに開発した両親媒性ヤヌスナノ粒子を用いることで、多剤耐性グラム陰性菌に対する抗菌薬の効果(感受性)を回復させることに成功しました。
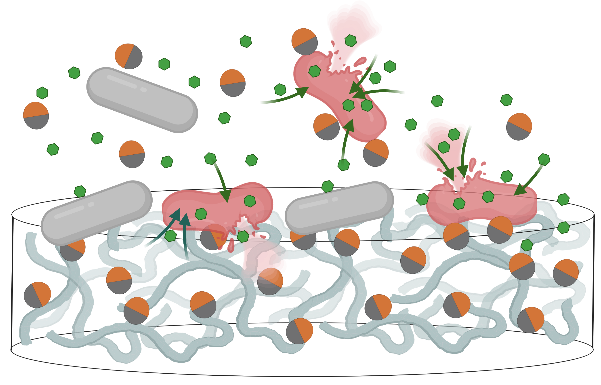
本研究で用いられたヤヌスナノ粒子は、粒子表面に役割の異なる2つの”顔”を有しており、一方が疎水性(水を嫌う性質)、もう一方が多価カチオン性(水中で電荷を使って結合する性質)という非対称の二面構造を有しています。この構造により細菌の外膜と強く相互作用し、抗菌薬の透過性を高めることで、抗菌薬の効果を飛躍的に向上させました。
特に、標準的な抗菌薬が効かず、WHOに「最優先の脅威菌」として指定され問題となっている、多剤耐性臨床分離株 Acinetobacter baumannii(アシネトバクター・バウマニ)においても、抗菌薬の感受性を大きく回復させることが確認されました。また、ヤヌスナノ粒子を寒天ゲルに組み込むことで、細菌との接触を安定化する新たな評価システムを構築し、今後の抗菌材料への応用の可能性も示しました。
本研究成果は2025年11月26日に米国科学誌『Nano Letters』(オンライン)に掲載されました。
本研究は、材料化学と微生物学を融合した国際共同研究により、単一分野では到達できなかった新しい発想を実証した成果です。多剤耐性菌感染症は世界的に深刻化しており、医療現場で大きな問題となっています。本研究で示した両親媒性ヤヌス型ナノ粒子は、既存の抗生物質の効果を回復させる新たな戦略であり、耐性獲得が起こりにくい点でも社会的インパクトの大きい技術であると考えています。本成果が将来的な耐性菌対策の一助となることを期待しています。
研究の背景
世界的に抗菌薬に対する耐性菌感染症数が増加しており、とりわけ Acinetobacter baumannii (アシネトバクター・バウマニ)や Escherichia coli(大腸菌)といったグラム陰性菌は、強固な外膜と多剤排出システムを有することから、薬が効きにくく、極めて深刻な脅威となっています。これらの細菌の多くはすでに複数の抗菌薬に耐性を示しており、一部の株は現在治療に用いられるほぼ全ての薬に耐性を獲得しています。耐性は、抗菌薬の標的に対する変異や、抗菌薬の分解・修飾、膜透過性の変化、さらには細胞外へ薬剤を能動的に排出する排出ポンプの過剰発現などによって生じることが分かっています。その結果、かつてよく用いられていた抗菌薬の効果が急速に失われつつあります。
既存抗菌薬の有用性を維持するためには、抗菌薬と併用して耐性菌に対する殺菌効果を回復させることができる、新しいアジュバント化合物の開発が喫緊の課題となっています。この課題に対処するため、私たちは独自の「二面性(両親媒性)構造」を持つヤヌスナノ粒子を開発しました。これは、細菌膜と相互作用してその構造を弱体化させ、複数の抗菌薬クラスの活性の増強を目指したものです。
研究の内容
研究チームは、疎水性の半球と多価カチオン性の半球から構成される、独自の両親媒性ヤヌスナノ粒子を開発しました。この設計により、ヤヌスナノ粒子はグラム陰性菌の細胞膜に付着し、膜構造を変形させ、併用する抗菌薬の取り込みおよび活性を増強することが可能となります。ごく低濃度では、ヤヌスナノ粒子単独では細菌を殺傷しませんが、抗菌薬と併用することで相乗的に作用します。
<主な成果>
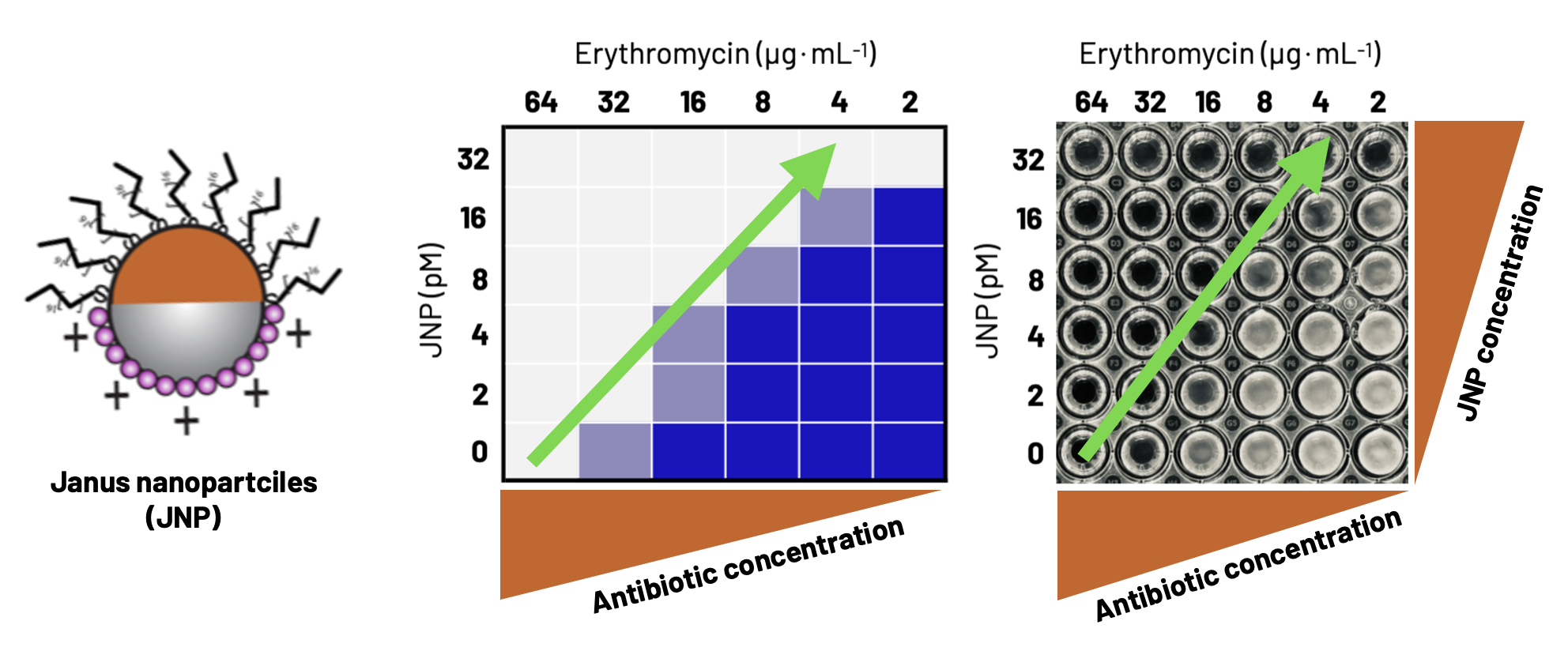
• エリスロマイシン、ノボビオシン、リファンピシン、カナマイシン、エチジウムブロマイド、クロキサシリンなど、複数の抗菌薬とヤヌスナノ粒子との間で強い相乗効果を確認しました。
• 抗菌薬の種類に応じて、必要な抗菌薬濃度が複数の細菌種で100倍以上低減しました。
• 対称構造のナノ粒子では相乗効果が見られなかったことから、ヤヌスナノ粒子の非対称性が機能発現に必須であることを示しました。
• 運動性を有する大腸菌などに確実に接触でき、β-ラクタム系のような作用発現が遅い抗菌薬でも一貫した効果増強が可能な、寒天ゲル内に埋め込んだヤヌスナノ粒子システムを新たに開発しました。これにより、抗菌コーティングや創傷被覆材など臨床応用の可能性が示されました。
本研究成果が社会に与える影響(本研究成果の意義)
本研究は、遺伝子学的および生化学的標的化に依存しない、マテリアル化学に基づく新しい抗菌薬活性化戦略を示すものです。ヤヌスナノ粒子は細菌膜との物理的相互作用を介して作用するため、耐性獲得が起こりにくく、多くの既存抗菌薬と相乗効果を発揮でき、アジュバントとして併用することで、既存薬の有効寿命を延長します。
さらに、ヤヌスナノ粒子を埋め込んだ寒天ゲルは、抗菌コーティングや薬剤送達システムなど、多剤耐性菌感染を抑制する新たな臨床応用への展開を可能にすることが期待されます。
特記事項
本研究成果は11月26日に米国科学誌『Nano Letters』(オンライン)に掲載されました。
タイトル:“Amphiphilic Janus Nanoparticles Synergize with Antibiotics to Restore Susceptibility in Drug-Resistant Gram-Negative Bacteria”
著者名:Martijn Zwama, Swagata Bhattacharyya, Nozomi Sakurai, Kunihiko Nishino, Yan Yu
DOI:10.1021/acs.nanolett.5c05337
本研究は、日本学術振興会(JSPS)科学研究費補助金、住友財団、日本財団・大阪大学感染症対策プロジェクト、文部科学省「物質・デバイス領域共同研究拠点」の共同研究プログラム、大阪大学グローバル展開研究プログラム(Global Expansion Research Program)、ならびに米国国立科学財団(NSF)の支援を受けて実施されました。
なお、本ナノ粒子技術に関しては特許出願も行っています。
用語説明
※1 多剤耐性菌
複数の抗生物質に対して抵抗性を示す細菌。特にグラム陰性菌は外膜のバリア性や薬剤排出ポンプ※5によって強い耐性を示す。
※2 グラム陰性菌
外膜と内膜の“二重の膜”をもつ細菌で、薬が中に入りにくい。グラム染色に陰性である細菌。多くの薬剤耐性菌がこのグループに属し、問題となっている。
例:E. coli(大腸菌)、Acinetobacter baumannii(アシネトバクター・バウマニ)
※3 ヤヌスナノ粒子
表面の左右(または上下)で異なる性質を持つ二面構造のナノ粒子。前後に2つの顔を持つローマ神話の双面神「ヤヌス(Janus)」にちなんで命名された。本研究では、片側が疎水性、もう片側が多価カチオン性という「両親媒性」を持ち、細菌の外膜に強く作用して膜透過性を高める。
※4 抗菌アジュバント
抗生物質そのものではなく、抗生物質の効果を高める補助剤のこと。ナノ粒子や阻害剤など、単独では細菌を殺さなくても、既存の抗生物質の効力を大幅に向上させる。
※5 薬剤排出ポンプ
細菌の膜に存在し、薬を菌体外に排出するポンプ。薬剤耐性の大きな原因であり、本研究のナノ粒子はこれらの防御を“物理的に弱める”役割を果たす可能性がある。

